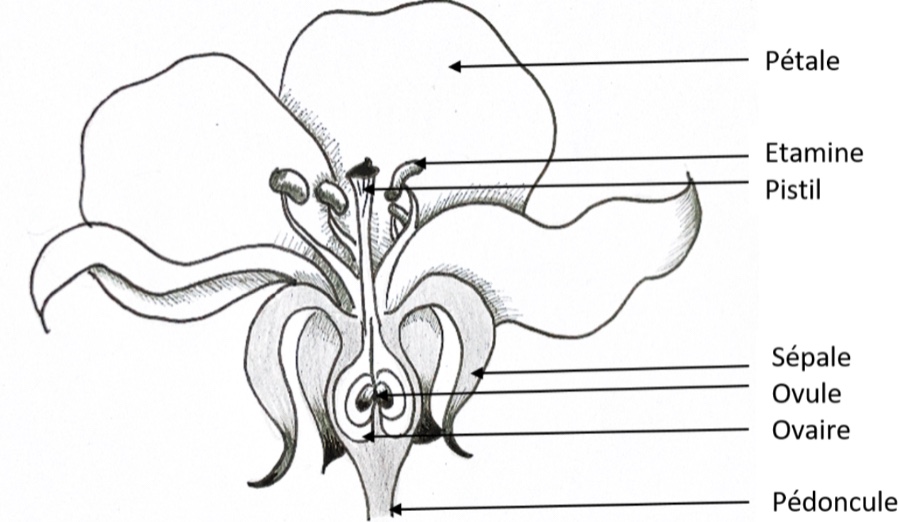
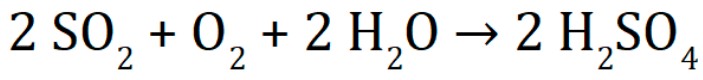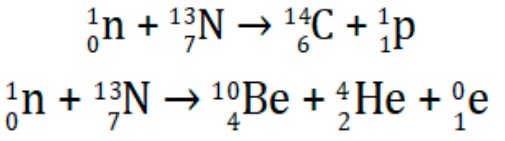Pieter BRUEGHEL L’ANCIEN, Le Dénombrement de Bethléem, 1566, huile sur bois, L : 1m64, Bruxelles, Musée des Beaux-Arts de Belgique
Cet hiver j’avais envie de vous parler du Petit Âge glaciaire. Outre que cette période climatologique m’intéresse particulièrement -arrêtez de me regarder comme ça ! On est tous à l’École, on a tous des passions un peu (très) bizarres !-, je trouvais que cela rentre parfaitement dans le thème Chaos -non Billy, ce n’est pas juste un article que j’ai essayé de placer où je le pouvais, alors cesse de me dénigrer ainsi !
Cependant -et à la demande expresse de Billy- je vais tout de même vous expliciter cette dernière impression, histoire de ne pas vous laisser sans rien. Premièrement, notez que la météorologie est (vraisemblablement) basée sur la théorie du chaos, que je ne vais pas essayer d’expliquer ici parce que… parce que. Et puis allez sur Wikipédia si ça vous plaisir ! Ensuite, il faut voir le chaos que provoque ce Petit Âge glaciaire : on parle quand-même de la disparition de trente à cinquante pourcents de la population européenne, notamment du fait des famines ! Et non ce n’est pas une explication tirée par les cheveux visant à faire entrer cet article dans le thème !
Tout d’abord, qu’est-ce que le Petit Âge glaciaire ? Il s’agit d’une période de désordre et de refroidissement climatique s’étendant selon les spécialistes environ du début du XIIIe siècle au milieu du XIXe siècle. On admet, d’après les reconstitutions de températures, une perte de moins de 1° C (cela paraît peu, mais c’est assez pour mettre le bazar apparemment) en moyenne sur toute la période. Mais ce refroidissement n’est pas uniforme et on peut en distinguer trois phases remarquablement plus fortes : de 1300 à 1380, dans le dernier tiers du XVIIe siècle puis enfin entre 1815 et 1860. A contrario, on relève des étés particulièrement chauds dans la moitié du XVIIIe siècle.
Cette période aux hivers souvent très froids et aux étés plutôt tièdes est marquée par des récoltes maigres, sources de famines, et des périodes de froids extrêmes (les fleuves comme la Seine gèlent complètement à l’hiver 1709, où ont atteint – 16° C à Paris, le vin du roi aurait même gelé dans son verre ! -note à soi-même : se faire du vin glacé cet été après le vin chaud de cet hiver …-). Les glaciers avancent partout : la calotte glaciaire s’étend en Atlantique dès 1250, provoquant la fin de la colonie norvégienne au Groenland faute de ravitaillement (elle disparaît vers 1400), des villages sont engloutis par les glaces un peu partout dans les Alpes, …
Pour autant, ce Petit Âge glaciaire est marqué par de grandes avancées techniques ! En effet, l’être humain est une espèce particulièrement adaptable. D’immense greniers sont construits pour stocker les récoltes meilleurs des années pour les périodes de famines, les moulins à vent remplacent peu à peu les moulins à eau souvent pris dans les glaces, le brise-glace est inventé à Amsterdam pour permettre l’approvisionnement de la ville, c’est l’invention des skis, raquettes et autres traîneaux en Europe, et surtout, SURTOUT, on note une très conséquente hausse de la production de BIÈRE ! -no fake, la raison est que cet alcool se conserve mieux que le vin à l’époque, et aussi que la vigne a besoin de plus de chaleur.
Mais parlons un peu de science voulez-vous ! Quelles sont les causes de ce Petit Âge glaciaire ?
Une première explication pourrait être l’activité volcanique explosive, très forte entre la fin du fin XVIe siècle et la fin du XVIIe siècle. Une éruption volcanique explosive envoie, pour peu qu’elle soit conséquente, de nombreux gaz dans les couches hautes de l’atmosphère. Ainsi, du dioxyde de soufre (SO2) parvient dans la troposphère où il réagit avec le dioxygène (O2) et l’eau (HéO) pour former de l’acide sulfurique (H2SO4) :
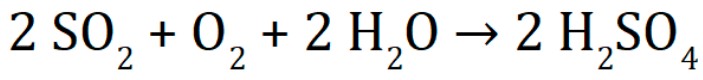
Ces gouttelettes d’acide sulfurique opacifient l’atmosphère et réfléchissent les rayons du soleil, qui ne parviennent donc plus jusqu’au sol. Cela provoque donc une baisse de température à la surface terrestre, ce que l’on appelle un hiver volcanique, mais aussi une hausse de température dans la haute atmosphère, modifiant les courants atmosphériques et provoquant ainsi des perturbations météorologiques. Cependant, ces aérosols retombent au sol un à trois ans après les plus grosses éruptions, et cela ne peut expliquer un refroidissement séculaire du climat.
Il faut donc chercher ailleurs, directement au niveau du soleil par exemple. En effet, loin d’être constant, l’éclairement du soleil varient selon un cycle d’environ onze ans ainsi que selon d’autres cycles séculaires et millénaires encore mal connus. Cette variation est le fait de changements au sein de son champ magnétique, sans doute issus de ce que l’on appelle la dynamo solaire. Cette théorie explique la création d’un champ magnétique par un un corps conducteur (le Soleil) parcouru par un courant électrique du fait de mouvements convectifs (des déplacement de matière fluide) au sein dudit corps. Cet effet dynamo et ses changements sont encore très mystérieux mais on en observe tout de même les effets sur le Soleil et sur Terre.
Ainsi, on peut remarquer sur le soleil des taches noires, les taches solaires. Elles sont issues de ces mouvements convectifs de matière au sein de notre étoile, et marquent des zones de plus faible chaleur. Cependant, si la chaleur, et donc l’éclairement, est moindre au niveau de ces taches, il augmente autour d’elles. Cela fait que, contre-intuitivement, plus il y a de taches solaires, froides, plus l’éclairement solaire est important. Ces taches sont observables (et, peu ou prou, observées) depuis l’invention du télescope en Hollande en 1608 et on remarque ce que l’on appelle de Grands minima (des périodes presque sans taches solaire, donc à éclairement moindre) lors des périodes plus froides d’après les témoignages (comme le Grand minimum de Maunder entre 1645 et 1715). Mais leur observation ne couvre pas tout le Petit Âge glaciaire, ainsi doit-on, pour l’étudier, se baser sur d’autres sources.
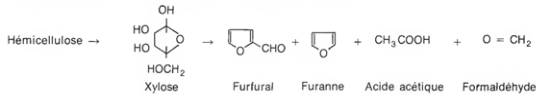
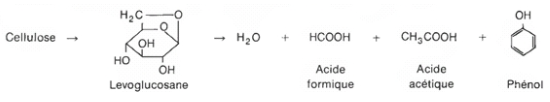
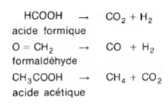
Et cela tombe bien, car on trouve sur terre des éléments très vieux dont la production est directement liée au rayonnement solaire : les cosmonucléides. Ça ne vous dit rien ? Pourtant je vous assure que nous, en archéologie, on en connaît très bien un : le carbone 14 ! Et oui, vous ne vous êtes jamais demandés pourquoi se formait cet isotope de l’élément carbone (C) ? Et bien moi si -c’est qu’on s’ennuie à l’hôpital psychiatrique avec Billy quand-même… sans offense Billy-, et en voici l’explication. Tout d’abord, le carbone a, à son état stable, 13 nucléons (protons et neutrons réunis, dans le noyau) et un numéro atomique (nombre d’électrons autour du noyau ou de protons dans le noyau, ce qui revient au même) de 6. Mais il est possible de créer des isotopes (souvent instables) d’un même élément, c’est à dire des atomes avec plus ou moins de neutrons qu’à la normale mais avec le même nombre de protons et d’électrons. C’est ce qui se passe avec le carbone 14, qui à 14 nucléons (donc 8 neutrons au lieu de 6 ou 7 normalement). Ces isotopes se désintègrent est cela permet des datations mais ce sera le sujet d’un autre apARTé scientifique. Pour ce qui est de cosmonucléides, il s’agit d’isotopes créés par l’interaction entre des atomes et les rayons cosmiques (pour leur plus grande part issus du Soleil). En bref, ces rayons constitués de diverses particules qui agissent dans la très haute atmosphère sur des atomes terrestres. On se penchera sur la formation des deux isotopes principalement utilisés dans ces études, le carbone 14 (observé dans les cernes des arbres) et le béryllium 10 (capturé par les glaces), dont voici les équations de formations * :
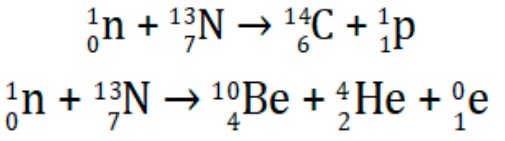
Mais pourquoi est-ce que je vous explique tout ça ? Et bien parce que, comme je l’ai dit précédemment, les variations d’éclairement solaire provoquent des variations dans la production de cosmonucléides. En effet, une forte activité solaire provoque une augmentation, en plus de son éclairement, de son éjection de plasma dans l’espace. Ces éjections de plasma sont dues à la violence des fusions ayant lieu à la surface du Soleil (de l’hydrogène fusionnant en deutérium, un isotope de l’hydrogène) qui provoque l’expulsion des résidus de ses fusions (particules, noyaux d’hélium, …), formant ce que l’on appelle le vent solaire (celui que l’on observe aux pôles sous la forme d’aurores boréales). Or, plus ce vent solaire est fort, plus il balaye les particules apportées par le rayonnement du Soleil loin dans le système solaire. De ce fait, on remarque une baisse de la formation de cosmonucléides, piégés alors sur Terre en moins grande quantité et dont on peut enfin noter les variations de concentration et en faire des conclusions sur l’état de l’intensité solaire, et donc du climat, lors des siècles précédents. Les chercheurs remarque donc une perte de température moyenne sur l’ensemble de la période oscillant entre 0,25 et 0,95° C suivant les valeurs retenues. Ils notent d’ailleurs quatre minima d’intensité solaire durant le Petit Âge glaciaire : le minimum de Wolf (1300-1350), le minimum de Spörer (1400-1600), le minimum de Maunder (1645-1715) et le minimum de Dalton (1790-1820) (notés W, S, M et D sur le schéma suivant). Ainsi qu’un pic d’intensité solaire au milieu du XVIIIe siècle, période aux étés particulièrement chauds si vous vous souvenez bien.
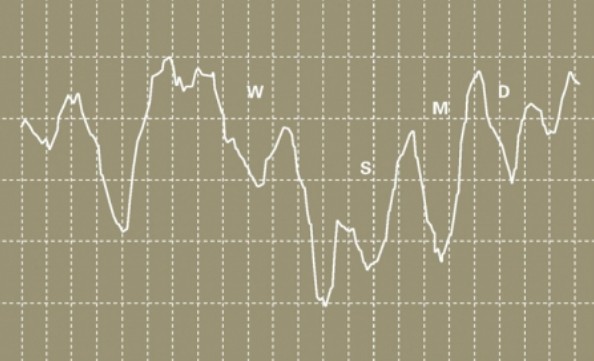
Évolution de l’éclairement solaire, reconstituée à partir de la production de béryllium 10 observée dans les glaces des forages de l’Antarctique par E. Bard (2000) depuis 850 de l’ère chrétienne.
Enfin, je vais vous faire part d’une autre possible explication du phénomène, qui si elle n’en explique bien entendu toute l’ampleur, me semble très intéressante. Une étude menée par quatre géographes de l’University College de Londres et de l’université de Leeds semble indiquer que les pandémie ayant décimé les peuples d’amérindiens (jusqu’à 90 %, soit un passage de 60 à 6 millions de personnes) pourrait avoir un lien avec le Petit Âge glaciaire. En effet, l’abandon de leurs terres par ces peuples provoqua la formation 56 millions d’hectares de savanes et de forêts. Cette hausse exponentielle de capteurs de CO2 (par photosynthèse) aurait provoqué un retrait de ce dernier élément équivalent à plusieurs dizaines de milliards tonnes. L’absorption de ce gaz à effet de serre pourrait donc être, en moindre partie, une cause de la chute des températures (ou plutôt de son intensification). Cet exemple est assez intéressant car il montre l’impact de l’être humain sur le climat, même avant l’ère industrielle, et cela prouve bien qu’un fait semblant complètement à part d’un sujet peu tout à fait, d’une façon ou d’une autre, l’avoir influencé.
Mais parlons d’art maintenant ! Non parce que c’est quand-même le but de cette rubrique au départ…
Pour commencer par le plus logique, la peinture hollandaise du XVIIe. On voit tous à peu près ces grands paysages enneigés des toiles de Brueghel l’Ancien pour ne citer que lui. Et bien on peut tout à fait se poser la question d’une potentielle représentation des refroidissements causés par le Petit Âge glaciaire. C’est ainsi que Les chasseurs dans la neige (1565) ou Le dénombrement de Bethléem (1566) sont peint pendant et juste après l’hiver de 1565, particulièrement rude. Pour autant, il faut replacer ces créations dans leur contexte et ne pas tirer de conclusions hâtives. Car à cette époque, les Pays-Bas se séparent peu à peu de l’Espagne (le traité d’Utrecht, marquant la prise d’indépendance des Provinces-Unis vis-à-vis des Habsbourg, est signé en 1579, s’ensuit la guerre de Quatre-Vingt Ans). La région revendique donc peut-être une identité propre par la représentation d’un hiver froid typiquement hollandais et bien loin de l’Espagne torride et ensoleillée.

- Pieter BRUEGHEL L’ANCIEN, Les chasseurs dans la neige, 1565, huile sur bois, L: 1m62, Vienne, Kunsthistorischesmuseum
Pour ce qui est de la sculpture, on peut se rappeler les cours de Moyen Âge de Deuxième Année et le style parisien des années 1300 imitant des « drapés de laine » (remplaçant les drapés mouillés du XIIIe siècle) pour citer M. Meunier. Citons par exemple (et pour faire plaisir à ce dernier), les diverses statues dédiées à la collégiale d’Écouis par Enguerrand de Marigny en 1311, soit au tout début du Petit Âge glaciaire. Or, les températures plus basses n’auraient-elles pas eu un impact sur la mode vestimentaire (avec des habits de laine, plus chauds), et donc sur le style sculptural ? Après interrogation dudit professeur à ce sujet, il s’avère sceptique à l’idée mais ne balaye pas l’hypothèse d’un rapport de conséquence, serait-il partiel.

Sculpture de Sainte Véronique – Collégiale Notre-Dame d’Ecouis
Enfin, la musique aurait aussi subi un impact certain, avec les violons de Stradivarius, luthier crémonais oeuvrant de 1670 à 1737. Réputés exceptionnels, on a longtemps cherché l’origine de leur acoustique jugée parfaite avant de, peut-être, la trouver dans … la densité de leur bois. En effet, si ils ne sont en moyenne pas plus denses que les violons modernes, ces violons anciens possèdent une plus grande homogénéité de densité au sein des pièces de bois les composant. Or, cette plus grande homogénéité peut s’expliquer par une croissance plus lente du bois, courante lors de périodes plus froides comme le minimum de Maunder de 1645 à 1715 par exemple ! Cependant, cela signifierait que les violons de tous les luthiers de Crémone serait de cette même qualité, ce qui est faux. De plus, la supposée supériorité des Stradivarius est plus que controversée.
Bien, nous voilà à la fin de cet article après ce petit marathon scientifique. Ça fait du bien de se remettre en jambes après les vacances, hein Billy ? Certes l’étude de l’impact sur l’art du Petit Âge glaciaire n’est que peu concluante, mais il reste intéressant de voir l’impact du climat sur les populations humaines et, peut-être, leurs productions artistiques. Cela laisse tout de même pensif en cette période de brusques changements climatiques.
Raphaël VAUBOURDOLLE
* Pour les particules : n (neutron), p (proton) et e (positron) ; pour les atomes : N (azote), C (carbone), Be (béryllium) et He (hélium).